EPHEDRINE AGUETTANT 3 mg-ml, solution injectable en seringue préremplie, boîte de 5 seringues préremplies de 10 ml
Retiré du marché le : 17/11/2009
Dernière révision : 09/03/2020
Taux de TVA : 2.1%
Laboratoire exploitant : AGUETTANT
· Traitement de l'hypotension au cours de l'anesthésie générale et de l'anesthésie loco-régionale qu'elle soit rachidienne ou péridurale et pratiquée pour un acte chirurgical ou obstétrical.
· Traitement préventif de l'hypotension au cours de l'anesthésie rachidienne pour un acte chirurgical ou obstétrical.
Ce médicament ne doit jamais être utilisé en cas de :
· hypersensibilité au principe actif ou à l'un des excipients mentionnés à la rubrique Liste des excipients.
· en association avec d'autres sympathomimétiques indirects comme la pseudoéphédrine, le méthylphénidate, le bupropion, la cafedrine, la theodrenaline.
· en association avec des sympathomimétiques alpha,
· en association avec des IMAO irréversibles
Mises en garde spéciales
La prudence est recommandée chez les patients susceptibles d'être particulièrement sensible aux effets de l'éphédrine, notamment en cas d'hyperthyroïdie.
Une attention particulière est également requise chez des patients atteints de pathologies cardiovasculaires telles que :
· maladie cardiaque ischémique,
· arythmie ou tachycardie,
· pathologies vasculaires occlusives incluant l'artériosclérose,
· hypertension,
· anévrismes.
Les douleurs angineuses peuvent être aggravées chez des patients souffrant d'angine de poitrine.
Les patients atteints de diabète, de glaucome à angle fermé et d'hypertrophie de la prostate doivent également faire l'objet d'une attention particulière lorsque l'éphédrine leur est administrée.
Précautions d'emploi
L'éphédrine doit être utilisée avec précautions chez les patients ayant des antécédents cardiaques.
Sportifs: attention cette spécialité contient un principe actif pouvant induire une réaction positive des tests pratiqués lors des contrôles anti-dopage.
Ce médicament contient 33,9 mg de sodium par seringue, ce qui équivaut à 1,7% de l'apport alimentaire quotidien maximal recommandé par l'OMS de 2 g de sodium par adulte.
Les effets indésirables sont classés par système organe et par fréquence selon la règle suivante :
Très fréquent : > 1/10; fréquent : (≥1/100 à <1/10); peu fréquent: (≥1/1000 à <1/100); rare: (≥1/10000 à <1/1000); très rare : (<1/10000); fréquence indéterminée : (ne peut être estimé sur la base des données actuellement disponibles).
· Affections hématologiques et du système lymphatique
Indéterminé : modifications de l'hémostase primaire.
· Affections du système immunitaire
Indéterminé : hypersensibilité.
· Affections psychiatriques
Indéterminé : confusion mentale, anxiété, dépression.
· Affections du système nerveux
Indéterminé : nervosité, irritabilité, insomnie, tremblements.
· Affections oculaires
Indéterminé : crises de glaucome à angle fermé.
· Affections cardiaques
Indéterminé : palpitations, hypertension, tachycardie, arythmie cardiaque, douleurs angineuses, bradycardie réflexe, arrêt cardiaque. Un syndrome de Takotsubo (cardiomyopathie de stress) peut survenir.
· Affections vasculaires
Indéterminé : hémorragie cérébrale.
· Affections respiratoires, thoraciques et médiastinales
Indéterminé : dyspnée, oedème pulmonaire
· Affections du rein et des voies urinaires
Indéterminé : rétention urinaire
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Grossesse
Les études effectuées chez l'animal ont mis en évidence un effet tératogène.
En clinique, les résultats des études épidémiologiques menées sur des effectifs limités de femmes semblent exclure un effet malformatif particulier de l'éphédrine.
En cas d'abus ou d'utilisation chronique d'amines vasoconstrictrices, des cas isolés d'hypertension maternelle ont été rapportés.
Toutefois, il n'existe pas actuellement de données en nombre suffisant pour affirmer la réalité d'une foetotoxicité de l'éphédrine lorsqu'elle est administrée pendant la grossesse.
De par son effet sympathomimétique, une augmentation, de la fréquence et de la variabilité du rythme cardiaque foetal peut être observée.
En conséquence, l'utilisation de l'éphédrine ne doit être envisagée au cours de la grossesse que si nécessaire.
Allaitement
Il n'existe pas de données concernant le passage de l'éphédrine dans le lait maternel. Cependant, compte-tenu des modalités d'administration de ce médicament, l'allaitement est possible.
Associations contre-indiquées
· Autres sympathomimétiques indirects (bupropion, cafédrine, méthylphénidate, pseudoéphédrine, théodrénaline).
Risques de vasoconstriction et /ou de crises hypertensives.
· Sympathomimétiques alpha (voies orale et/ou nasale).
Risque de vasoconstriction et/ou de poussées hypertensives.
· IMAO irréversibles
Hypertension paroxystique, hyperthermie pouvant être fatale. Du fait de la durée d'action de l'IMAO, cette interaction est encore possible 15 jours après l'arrêt de l'IMAO.
Associations déconseillées
· Alcaloïdes de l'ergot de seigle dopaminergiques
Risque de vasoconstriction et/ou de poussées hypertensives.
· Alcaloïdes de l'ergot de seigle vasoconstricteurs
Risque de vasoconstriction et/ou de poussées hypertensives.
· IMAO-A réversibles, y compris linézolide et bleu de méthylène
Risque de vasoconstriction et/ou de poussées hypertensives.
· Antidépresseurs tricycliques (imipraminiques)
Hypertension paroxystique avec possibilité de troubles du rythme (inhibition de l'entrée de l'adrénaline ou de la noradrénaline dans la fibre sympathique).
· Antidépresseurs sérotoninergiques-noradrénergiques (minalcipran, sibutramine, venlafaxine)
Hypertension paroxystique avec possibilité de troubles du rythme (inhibition de l'entrée de l'adrénaline ou de la noradrénaline dans la fibre sympathique).
· Anesthésiques volatils halogénés
Trouble du rythme ventriculaire grave par augmentation de l'excitabilité cardiaque.
Posologie
Adulte
La dose est de 3 à 6 mg, répétée en fonction des besoins toutes les 5 à 10 min.
La dose totale doit être inférieure à 150 mg par 24 heures.
L'absence d'efficacité doit faire reconsidérer le choix du traitement.
Population pédiatrique
La voie d'administration est intraveineuse.
La dose est de 0,1 à 0,2 mg/kg toutes les 4 à 6 heures.
Mode d'administration
L'Ephédrine devra être uniquement utilisée par ou sous la responsabilité du médecin anesthésiste.
Voie injectable.
Perfusion intraveineuse ou bolus IV. La voie d'administration varie selon l'état du malade, en fonction du poids et des thérapeutiques complémentaires.
Durée de conservation :
3 ans.
Après ouverture du blister: le produit doit être utilisé immédiatement.
Précautions particulières de conservation :Conserver le blister dans l'étui à l'abri de la lumière.
Vérifier un éventuel changement de couleur et/ou une éventuelle formation de précipité, de complexe insoluble ou de cristaux.
En cas de surdosage, des nausées, des vomissements, de la fièvre, une psychose paranoïaque, des troubles du rythme ventriculaire et supraventriculaire, une hypertension, une dépression respiratoire, des convulsions et un coma peuvent être observés.
La dose létale chez l'homme est de l'ordre de 2 g correspondant à des concentrations sanguines de l'ordre de 3,5 à 20 mg/l.
Classe pharmacothérapeutique : ADRENERGIQUES ET DOPAMINERGIQUES, code ATC : C01CA26.
L'éphédrine est une amine sympathomimétique agissant directement sur les récepteurs alpha et bêta et indirectement en augmentant la libération de noradrénaline par les terminaisons nerveuses sympathiques. Comme tout agent sympathomimétique, l'éphédrine stimule le système nerveux central, le système cardiovasculaire, le système respiratoire, et les sphincters digestifs et urinaires. L'éphédrine est également un inhibiteur de la monoamine oxydase (MAO).
L'excrétion est dépendante du pH urinaire :
· de 73 à 99% (moyenne : 88%) dans l'urine acide,
· de 22 à 35% (moyenne : 27%) dans l'urine alcaline.
Après administration orale ou parentérale, l'éphédrine est excrétée sous forme inchangée dans l'urine à 77%.
La demi-vie est dépendante du pH urinaire. Quand l'urine est acidifiée à pH = 5, la demi-vie est de 3 heures, quand l'urine est alcalinisée à pH = 6,3, la demi-vie est approximativement de 6 heures.
Sans objet.
Sans objet.
Attention à bien respecter le protocole pour l'utilisation de la seringue.
La seringue pré-remplie est à usage unique, après la première utilisation tout le produit non utilisé doit être jeté.
Le contenu du blister non ouvert et non endommagé est garanti stérile, et par conséquent il ne doit être ouvert qu'au moment de l'utilisation.
En utilisant une technique aseptique, ÉPHÉDRINE AGUETTANT 3 mg/mL, solution injectable en seringue préremplie peut être utilisée sur un champ stérile.
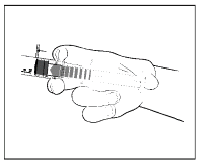 | 1) Retirer la seringue pré-remplie du blister stérile. |
| 2) Presser la tige du piston pour libérer le joint, car la stérilisation du produit fini a pu entraîner une adhérence des lèvres du joint sur le corps de la seringue. | |
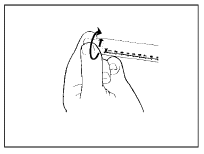 | 3) Dévisser l'embout protecteur en s'assurant de ne pas contaminer par contact l'embout luer de la connexion de la seringue. |
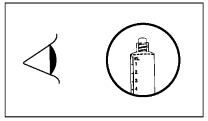 | 4) Vérifier que l'embout de scellage a bien été totalement retiré. |
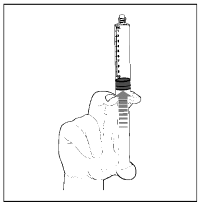 | 5) Purger l'air de la seringue en poussant légèrement le piston. |
| 6) Connecter la seringue à la voie d'accès IV. Pousser le piston pour injecter le volume requis | |
| 7) Après utilisation, éliminer la seringue selon les pratiques en vigueur dans votre établissement. |
Liste I
Médicament réservé à l'usage hospitalier.
Usage en situation d'urgence selon l'article R 5121-96 du code de la santé publique.
Solution injectable.
pH = 4,5 à 5,5
10 ml en seringue préremplie (verre type I) ; boîte de 5.
Chlorhydrate d'éphédrine......................................................................................................... 3 mg
Pour 1 ml
Une seringue préremplie de 10 ml contient 30 mg de chlorhydrate d'éphédrine.
Excipient(s) à effet notoire : sodium
Chaque ml de solution injectable contient 3,39 mg de sodium, équivalent à 0,15 mmol. Chaque seringue préremplie de 10 ml contient 33,9 mg de sodium, équivalent à 1,5 mmol.
Pour la liste complète des excipients, voir rubrique Liste des excipients.
Chlorure de sodium, acide citrique monohydraté, citrate de sodium, acide chlorhydrique ou hydroxyde de sodium, eau pour préparations injectables.
